北京时间10月25日,浙江大学医学院郭江涛课题组和基础医学系Dante Neculai教授团队的两项科研成果在国际顶尖杂志《科学》上刊登。
这两项重大成果解析了氯-钾共转运蛋白的结构,揭示了两个重要蛋白NOD1和NOD2的奥秘,为治疗癫痫和炎性肠病提供新思路。
耗时两年
拍出钾—氯共转运蛋白清晰的结构照片
人体细胞内的钾、钠、氯等离子稳态是受到严格调控的,离子稳态一旦失衡,就会导致高血压、抑郁、癫痫等一系列疾病。在细胞膜上,有一类被称为阳离子—氯离子共转运蛋白的蛋白质,它们可以带着离子进入和离开细胞,从而有效调控细胞内的离子稳态。

△团队成员郭江涛、叶升和刘斯在讨论课题
浙江大学医学院郭江涛课题通过长期的研究,解析了其中一个成员钾—氯共转运蛋白KCC1的结构。
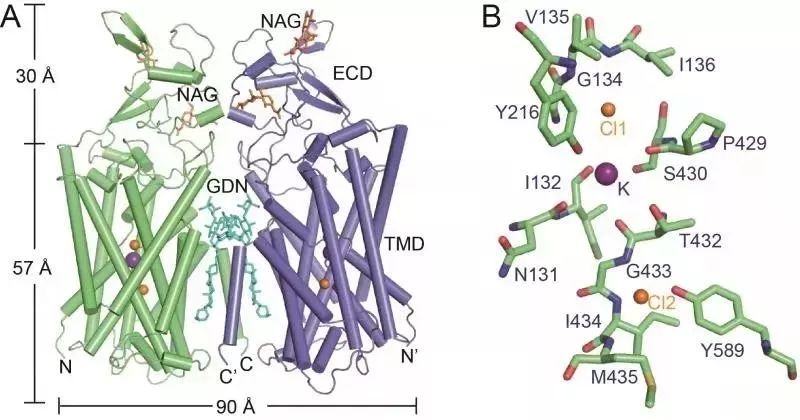
△图为人源KCC1的结构
但是解析钾—氯共转运蛋白KCC1的结构并不容易,为了给给它拍出一张可以清晰地看清三维结构的“好照片”,课题组花费了两年的时间。“拍到理想的照片真可谓一波三折,研究从2017年就开始了。但真正拿到高分辨结构已经是2019年初了。” 郭江涛告诉记者,“生物大分子样品对曝光十分敏感,电子的辐射会让其受损,拍照只能在曝光时间短、剂量低的情况下进行。”

△团队成员在分析结构数据
为了减少电子对蛋白的辐射损伤,蛋白样品需要的冷冻环境下进行数据收集。为了获得更清晰的画面,科研人员在8秒时间内连续拍摄40张照片,形成一个“微电影”,再通过图像处理将其“叠加”成一张照片。课题组从3000部“微电影”中,挑出了一两百万个蛋白颗粒进行数据处理。经过层层筛选,最终用十万个左右的高质量的蛋白颗粒进行高分辨率三维重构。
为治疗癫痫等提供新思路
这项研究成果,含金量在哪里?郭江涛说,KCC功能很重要,但是,想要做这个实验不容易。上世纪80年代全球就有科研人员在做这方面的研究,但是,共转运蛋白获得不容易,另一个就是这类较小分子量的膜蛋白高分辨率结构解析结构很难。“我们这次的成功,也是基于冷冻电镜技术的发展,才能够完成结构解析,将这些分子看清楚。”
郭江涛说,接下去,团队将朝着如何调控小分子的方向去努力,“这样有助于今后临床或制药更直接地用于治疗高血压、癫痫等疾病。”
NOD蛋白 先天性免疫的重要识别受体
先天性免疫反应是人体防御外来病原体和应激物的第一道防线。胞质中的NOD蛋白就是在血液和小肠这两大系统中的重要模式识别受体,其家族中的NOD1和NOD2是抗细菌免疫的关键模式识别受体,它们通过识别细菌胞壁成分肽聚糖来介导免疫应答信号途径活化发挥重要作用。
Dante Neculai教授团队研究发现,NLR家族的两个重要受体蛋白NOD1和NOD2能够在棕榈酰转移酶的作用下发生棕榈酰化修饰,从而介导细菌性炎症信号通路的发生。

△Dante Neculai教授团队
很长一段时间内,科研人员认为,NOD1和NOD2原本就像两个“哨兵”,主要在细胞膜这个“城墙”内的细胞质中工作。尼古拉·但丁教授团队发现,通过棕榈酰转移酶,可以把两个“哨兵”贴着“城墙”工作,从而可以第一时间发现汇报敌情,激活炎症通路,招募血液中更多的白细胞,去黏附在损伤部位,或吃掉病菌。
为治疗炎症性肠病提供新思路
在全球范围内,炎性肠病每年会造成成千上万人的死亡。近30年来,我国该病发病率也有不断攀升的趋势。

△Dante Neculai指导团队成员分析结果
Dante Neculai教授团队的研究发现可以在临床上为遗传性肠炎提供诊断的新标志。未来还有望通过设计治疗方案,开发潜在化合物让蛋白的功能恢复,从而缓解或者治愈炎症性肠病。

综合来源|中国蓝新闻客户端 青年时报 浙江大学公众号
责编|孙宇
编辑|江翊骐